BNCTの今
世界のBNCTをリードする日本の基礎・臨床研究と技術開発
BNCTでは新規ホウ素化合物の開発とともに、既存の化合物の適応を拡大する基礎研究や効果的な使用法の開発研究が重要になります。ホウ素化合物は微視的分布が複雑で、正常組織を構成する細胞種によってホウ素の集積、線量が異なります。各々の細胞種の損傷が組織の損傷全体にどの様な割合で寄与するのかは、放射線生物学研究でも明らかになっていません。そのため、BNCTでは原則として血液中のホウ素濃度と、組織に照射された中性子フルエンスを基に仮想の線量を計算し、その線量にBPAやBSHの実効RBEとでもいうべき変換係数を乗じてX線等価線量を計算しています。この係数はCBE係数と呼ばれ動物実験で求められています。わが国の研究者により皮膚に対するBPA、肝細胞に対するBPA、BSHの値が決定され、悪性黒色腫と肝臓がんのBNCTが可能となりました。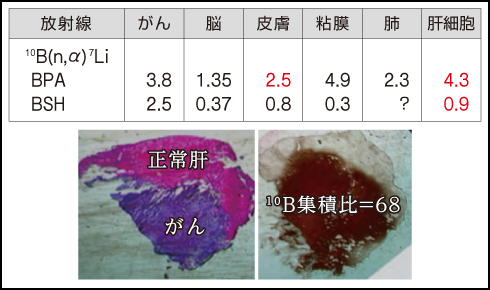
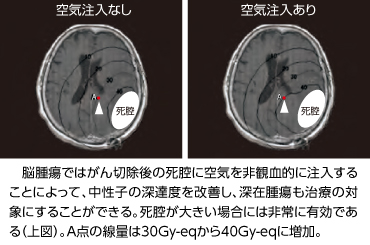 ホウ素化合物のがんへの選択的集積を得るために、京大炉グループKURの研究者等によってIVR(Interventional Radiology:画像下治療)技術の応用が考案されました。実験肝臓がんにIVR技術の応用でBSHを選択的に閉じ込めると約70倍の濃度比が達成されました。頭頸部がんでは腫瘍栄養動脈経由の超選択的ホウ素化合物投与も試みられています。
ホウ素化合物のがんへの選択的集積を得るために、京大炉グループKURの研究者等によってIVR(Interventional Radiology:画像下治療)技術の応用が考案されました。実験肝臓がんにIVR技術の応用でBSHを選択的に閉じ込めると約70倍の濃度比が達成されました。頭頸部がんでは腫瘍栄養動脈経由の超選択的ホウ素化合物投与も試みられています。
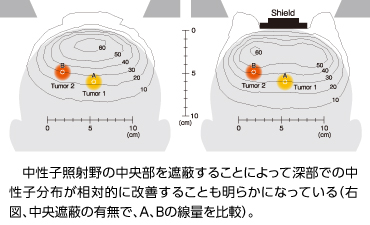 中性子はX線や重荷電粒子線と異なって、生体組織に照射されると霧が広がるように拡散します。そのため、X線などの経験からは意外と思える手法で深部分布が改善できます。
中性子はX線や重荷電粒子線と異なって、生体組織に照射されると霧が広がるように拡散します。そのため、X線などの経験からは意外と思える手法で深部分布が改善できます。
BNCTの実施の手順の一例
事前の診察、CT、MRIなどの画像検査、更にFBPA PETによる確認を経て実施されるBNCTの一般的手順を悪性脳腫瘍例で図示します。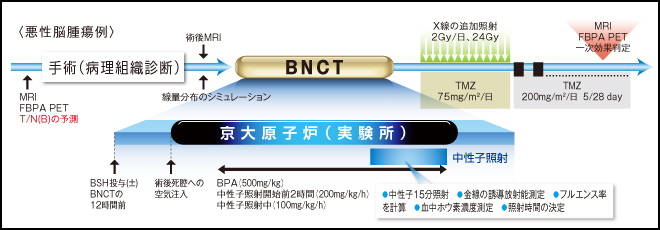
改良された熱中性子ビーム設備
米国でBNCTの臨床研究が失敗に終わった理由には、ホウ素化合物の脳腫瘍への選択的集積性の不足の他に、用いた中性子ビームの低品質、すなわち過度のガンマ線の混入がありました。わが国では改良された中性子ビームポートが臨床研究に用いられました。特にKURには、高純度の熱中性子を取り出せる重水熱中性子設備が附設されました。この設備はBNCTに特化したものではありませんでしたが、その熱中性子純度はCd比で5000、熱中性子フルエンス率で、6×109n/cm2・s、という世界最高水準の大変優れたものでした。
熱中性子利用から熱外中性子の利用へ
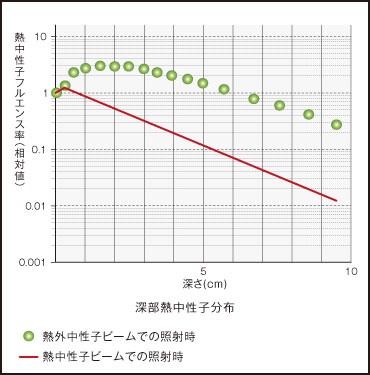 研究は1980年代の後半から再び盛り上がりを見せ、悪性神経膠腫、特に膠芽腫を対象に想定した基礎研究が進められました。照射された熱外中性子は体内の諸原子との反応で次第にエネルギーを失い、熱中性子に変わります。生体内で生成される熱中性子の深部分布は、2~3cmの深さで最大になり、表面との比は3程度です。
研究は1980年代の後半から再び盛り上がりを見せ、悪性神経膠腫、特に膠芽腫を対象に想定した基礎研究が進められました。照射された熱外中性子は体内の諸原子との反応で次第にエネルギーを失い、熱中性子に変わります。生体内で生成される熱中性子の深部分布は、2~3cmの深さで最大になり、表面との比は3程度です。
深部での熱中性子の減衰もやや緩やかです。そのため、熱外中性子ビームによる悪性脳腫瘍のBNCTでは照射施設での開頭手術が不要となります。1994年秋には米国がBNLの研究炉で熱外中性子ビームを用いて、非開頭でのBNCTを実施しました。わが国では、KUR附設の重水熱中性子設備を熱外中性子をも利用できる設備にする改造が1995年~1996年に行われました。ただ、熱中性子ビームによるBNCTへの執着が未だ強く、本格的に熱外中性子ビームが利用されるのは、今世紀の到来を待たねばなりませんでした。わが国ではKURに続いて、旧原研の研究炉においても設備の改造が行われました。
FBPA PETの登場
ホウ素化合物の集積が良好ながんでは、BNCTの効果が確実に期待できるため、そうしたがんの患者を事前の検査で選別できると効率の良い治療が可能になります。幸い、BPAは陽電子放出核種である18Fで標識でき、がんへの集積をPETで確認、更にがん対正常組織(血液)の18F放射能から集積比を予測することができます。このFBPA PETの事前検査に基づいた世界最初のBNCTは1994年2月にKURを用いて行われ、予測どおりの反応・効果を得ました。